一种新的合成基因控制系统
使用基于CRISPR蛋白质的方法,麻省理工学院的研究人员开发了一种新方法来精确控制哺乳动物细胞中产生的特定蛋白质的数量。
该技术可用于微调有用蛋白质的产生,例如用于治疗癌症和其他疾病的单克隆抗体,或细胞行为的其他方面。在他们发表在《自然通讯》上的新研究中,研究人员表明,该系统可以在多种哺乳动物细胞中发挥作用,结果非常一致。
“这是一个高度可预测的系统,我们可以预先设计,然后得到预期的结果,”前麻省理工学院研究科学家WilliamCWChen说。“这是一个非常可调的系统,适用于不同细胞类型的许多不同生物医学应用。”
现在是南达科他大学生物医学科学助理教授的陈与前麻省理工学院研究科学家列昂尼德盖杜科夫和博士后赖勇一起是这项新研究的主要作者之一。资深作者TimothyLu作为麻省理工学院生物工程、电气工程和计算机科学副教授领导了这项研究。
基因控制
许多治疗性蛋白质,包括单克隆抗体,都是在含有哺乳动物细胞的大型生物反应器中生产的,这些哺乳动物细胞经过工程改造以产生所需的蛋白质。几年前,麻省理工学院合成生物学中心的研究人员,包括卢的实验室,开始与辉瑞公司合作开发合成生物学工具,该工具可用于促进这些有用蛋白质的生产。
为此,研究人员针对他们想要上调的基因的启动子。在所有哺乳动物细胞中,基因都有一个与转录因子结合的启动子区域——转录因子是启动基因转录成信使RNA的蛋白质。
在之前的工作中,科学家们设计了合成转录因子,包括称为锌指的蛋白质,以帮助激活靶基因。然而,锌指和大多数其他类型的合成转录因子必须针对它们靶向的每个基因重新设计,这使得它们的开发具有挑战性和耗时。
2013年,Lu实验室的研究人员开发了一种基于CRISPR的转录因子,使他们能够更轻松地控制哺乳动物和酵母细胞中天然存在的基因的转录。在这项新研究中,研究人员着手在这项工作的基础上创建一个合成生物部分库,使他们能够传递转基因——一种细胞通常不表达的基因——并精确控制其表达。
“这个想法是拥有一个全谱合成启动子系统,可以从非常低到非常高,以适应不同的细胞应用,”陈说。
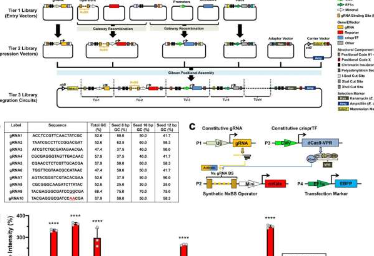
研究人员设计的系统包括几个组件。一个是要转录的基因,以及一个“操作符”序列,它由一系列人工转录因子结合位点组成。另一个成分是与那些操纵子序列结合的向导RNA。最后,该系统还包括一个与失活的Cas9蛋白相连的转录激活结构域。当这种失活的Cas9蛋白在合成启动子位点与引导RNA结合时,基于CRISPR的转录因子可以开启基因表达。
用于该合成系统的启动子位点被设计为与天然存在的启动子位点不同,因此该系统不会影响细胞自身基因组中的基因。每个操作员都包含2到16个指导RNA结合位点拷贝,研究人员发现他们的系统可以以与结合位点数量线性对应的速率启动基因转录,从而使他们能够精确控制产生的蛋白质量。
高一致性
研究人员在几种类型的哺乳动物细胞中测试了他们的系统,包括中国仓鼠卵巢(CHO)细胞,这些细胞通常用于在工业生物反应器中生产治疗性蛋白质。他们在CHO细胞和他们测试的其他细胞中发现了非常相似的结果,包括小鼠和大鼠成肌细胞(肌肉细胞的前体)、人类胚胎肾细胞和人类诱导的多能干细胞。
“该系统对不同细胞类型和不同靶基因具有非常高的一致性,”陈说。“这是思考通过高度可调、可预测的人工系统调节基因表达和细胞行为的一个很好的起点。”
在首次证明他们可以使用新系统诱导细胞产生预期数量的荧光蛋白后,研究人员表示他们还可以使用它来对称为JUG444的单克隆抗体的两个主要片段的生产进行编程。
研究人员还对CHO细胞进行了编程,以产生不同数量的人类抗体,称为抗PD1。当人类T细胞暴露于这些细胞时,如果产生更多的抗体,它们就会成为更有效的肿瘤细胞杀手。
他们说,尽管研究人员能够获得高产量的所需抗体,但仍需要进一步的工作将该系统整合到工业过程中。与工业生物反应器中使用的细胞不同,本研究中使用的细胞生长在平坦的表面上,而不是在液体悬浮液中。
“这是一个有望在工业应用中使用的系统,但首先我们必须将其应用于悬浮细胞,看看它们是否以相同的方式制造蛋白质。我怀疑它应该是相同的,因为没有理由它不应该,但我们仍然需要对其进行测试,”陈说。
推荐阅读
- 2021醉酒驾车的处罚标准是什么,醉酒驾驶怎么处罚2022年,醉酒驾车的处罚标准是什么
- 夏普空调维修服务(夏普空调维修)
- 笔记本电脑聚合物电池和锂电池哪个好,修复笔记本聚合物电池的方法与技巧
- 欧冠欧联杯分配名额,欧冠 欧联杯 欧协杯区别(中超积分榜总排名)
- 2020特岗教师报名时间(2020特岗教师报名时间表)
- 树莓派2和树莓派3的区别(树莓派2和树莓派3对比评测)
- 电脑版qq音乐有没有听歌识曲,电脑版QQ音乐如何听歌识曲
- Intel 酷睿2双核 T6570(intel 酷睿2双核 t6500)
- 自动挡的车怎么开详细教程,自动挡的车怎么开
- 经常刷机会对手机硬件有损害吗文章,经常刷机会对手机硬件有损害吗
- 东京奥运会田径破纪录有哪些选手,东京奥运会田径破纪录有哪些
- 2021安徽省农村信用社联合社招聘100人公告(安徽农村信用社招聘网站)
- 中国中药控股有限公司营销中心是骗子吗(国药集团是骗子)
- 如何更改电脑密码设置,电脑如何更改电脑键盘设置
- 三星安卓系统手机推荐(三星安卓系统手机)
- 铃木吉姆尼改装,吉姆尼改装
- 葛优老婆是谁,葛优老婆个人资料介绍
- 4种催熟香蕉的方法介绍,家庭用催熟生香蕉的方法
- 手机一边充电一边玩是否有害健康,手机一边充电一边玩是否有害
- 十大英语培训机构前10排名(国内英语培训机构前十名)
